ProSTEM adalah perusahaan pengolahan dan penyimpanan sel punca untuk terapi penyakit degeneratif. Keamanan pasien sangat diutamakan dalam pengolahan dan penyimpanan sel punca sesuai standar menurut Peraturan Kementrian Kesehatan No. 48 dan No. 50 tahun 2012, ISO 9001:2015 serta CPOB (Cara Pembuatan Obat yang Baik) oleh Badan POM RI untuk kualitas sel punca yang diproses dan disimpan dapat terjamin. Kualitas sel punca dapat diketahui dengan melakukan uji quality control yang meliputi pemeriksaan endotoksin, mycoplasma, karakterisasi sel, diferensiasi dan viabilitas sel yang berasal dari berbagai sumber sampel seperti darah perifer, bone marrow, darah tali pusat, jaringan tali pusat, lemak dan pulpa gigi. Fasilitas yang dimiliki ProSTEM telah memenuhi standar untuk aplikasi klinis.
Pengujian kemurnian produk merupakan salah satu indikator kualitas produk sel. Endotoksin adalah toksin/racun yang dihasilkan oleh bakteri gram negatif. Beberapa jenis dari bakteri tersebut dapat bersifat toksik bagi tubuh. Kandungan toksin pada endotoksin cukup berbahaya bagi manusia, yaitu dapat menyebabkan gangguan pernapasan, demam, gangguan fungsi organ, hingga kematian (1). Oleh karena itu, dibutuhkan pengujian analisis kualitatif untuk mendeteksi adanya kontaminasi endotoksin pada sel atau sampel yang diuji.
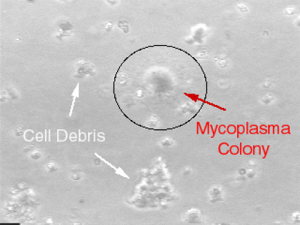
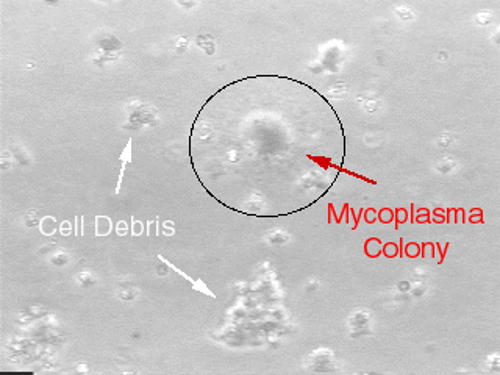
Gambar 1. Mycoplasma Colony (Sumber: https://unclineberger.org/)
Terdapat masalah penting lain yang perlu diperhatikan yaitu kontaminasi yang diakibatkan oleh mycoplasma. Mycoplasma merupakan prokariot yang memiliki lebih dari 100 jenis spesies, sehingga sering mangakibatkan gagalnya deteksi pada kultur sel. Pada proses kultur sel, mycoplasma dapat merusak kromosom sehingga morfologi dan fungsi sel berubah (2). Akibatnya, kualitas sel menurun dan tidak dapat digunakan.
Karakterisasi sel dengan immunophenotyping digunakan untuk mengidentifikasi produk sel terutama yang akan digunakan untuk aplikasi klinis. Identifikasi sel dibutuhkan untuk memastikan bahwa produk sel terapi mengandung populasi sel yang diinginkan dan tidak terdapat kontaminan. Hal tersebut penting untuk mengatasi kekhawatiran adanya kemungkinan sel berubah secara tidak terduga selama proses produksi (3). Karakterisasi pada sel punca dilakukan dengan mendeteksi molekul penanda yang terdapat pada permukaan sel. Deteksi Mesenchymal Stem Cell (MSC) dilihat melalui ekspresi molekul penanda CD90, CD73, CD105 dan lin negatif yang dimilikinya. Lin negatif merupakan gabungan dari molekul penanda CD45, CD34, 11b, 19 dan HLA-DR, sedangkan Endhotelial Progenitor Cell (EPC) dapat dideteksi dari ekspresi penanda CD34, CD45 dan CD133 (4).
Diferensiasi sel merupakan salah satu sifat sel punca, yaitu memiliki kemampuan untuk berubah menjadi sel lain(5). Potensi sel untuk berdiferensiasi dapat bermanfaat bagi terapi regeneratif karena sel tersebut dapat membentuk sel-sel yang diinginkan sehingga fungsi sel yang telah rusak dapat diperbaiki. Potensi kultur Mesenchymal Stem Cell (MSC) untuk aplikasi klinis dapat diketahui dengan melakukan uji diferensiasi sesuai dengan ketetapan International Society for Cellular Therapy (ISCT) tentang MSC, yaitu sel MSC mampu berdiferensiasi menjadi sel adiposa (lemak), sel kondrosit (tulang rawan) ataupun sel osteosit (tulang keras) sehingga sel tersebut dapat digunakan untuk terapi regeneratif.
Reference
- Li Y, Boraschi D. 2016. Endotoxin contamination: a key element in the interpretation of nanosafety studies. Nanomedicine. 11(3): 269-287.
- Ryan J. 2008. Endotoxins and Cell Culture. New York: Corning Incorporated.
- Carmen J, Burger SR, McCaman M, Rowley JA. 2012. Developing assays to address identity, potency, purity and safety: cell characterization in cell therapy process development. Regen Med. 7(1): 85-100.
- Wohlers I, Stachelscheid H, Borstlap J, Zeilinger K, Gerlach JG. 2009. The characterization tool: a knowledge-based stem cell, differentiated cell, and tissue database with a web-based analysis front-end. Stem Cell Research. 3:88-95.
- Riss TL, Moravec RA, Niles AL, Duellman S, Benink HA, Worzella TJ, Minor L. 2016. Cell Viability Assays. Bethesda: Eli Lily & Company
- Pamies D. 2017. Good cell culture practice for stem cells and stem cell derived models. ALTEX. 34(1): 95-132